การวิเคราะห์ซัลไฟต์ในน้ำผลไม้ด้วยเทคนิคดิฟเฟอเรนเชียลพัลส์โวลแทมเมทรี โดยใช้ขั้วไฟฟ้ากราฟีนชนิดพิมพ์สกรีนที่ไม่ผ่านการดัดแปลง
คำสำคัญ:
ซัลไฟต์, เครื่องดื่มน้ำผลไม้, ขั้วไฟฟ้ากราฟีนชนิดพิมพ์สกรีน, เทคนิคเคมีไฟฟ้า, อุปกรณ์ตรวจวัดแบบพกพาบทคัดย่อ
วัตถุประสงค์และที่มา : ปัจจุบันผู้บริโภคมีแนวโน้มที่จะให้ความสำคัญกับการดูแลสุขภาพเพิ่มมากขึ้น จึงส่งผลให้ความนิยมในการบริโภคน้ำผลไม้เพิ่มมากขึ้นด้วยเช่นกัน ทั้งนี้เนื่องจากน้ำผลไม้จัดเป็นแหล่งของวิตามินและแร่ธาตุที่มีประโยชน์ อย่างไรก็ตามน้ำผลไม้บรรจุกล่องมักมีการเติมวัตถุเจือปนอาหาร เช่น ซัลไฟต์ ซึ่งทำหน้าที่เป็นสารกันเสียและช่วยยืดอายุผลิตภัณฑ์ แต่หากบริโภคในปริมาณมากอาจเป็นอันตรายต่อสุขภาพได้ ดังนั้นจึงจำเป็นต้องมีวิธีการตรวจวิเคราะห์ซัลไฟต์ที่รวดเร็ว แม่นยำสูง และมีต้นทุนเหมาะสม ซึ่งมีความสำคัญอย่างยิ่งต่อการประกันคุณภาพ และความปลอดภัยของผลิตภัณฑ์อาหาร ด้วยเหตุนี้เทคนิควิเคราะห์ทางเคมีไฟฟ้า โดยเฉพาะเทคนิคดิฟเฟอเรนเชียลพัลส์โวลแทมเมทรี (DPV) ร่วมกับการใช้ขั้วไฟฟ้าชนิดพิมพ์สกรีน (Screen-Printed Electrode: SPE) จึงได้รับความสนใจอย่างกว้างขวาง เนื่องจากมีสภาพไวในการวิเคราะห์สูง ต้นทุนการวิเคราะห์ต่ำ ใช้สารตัวอย่างในการวิเคราะห์น้อย และเหมาะสำหรับการประยุกต์ใช้ในการวิเคราะห์ภาคสนาม โดยในงานวิจัยนี้เลือกใช้ขั้วไฟฟ้ากราฟีนชนิดพิมพ์สกรีนที่ไม่ผ่านการดัดแปลง ซึ่งมีสมบัติเด่นด้านการนำไฟฟ้า ความเสถียรทางเคมีและความแข็งแรงสูง ทั้งนี้วัตถุประสงค์ในการวิจัยนี้เพื่อพัฒนา และประยุกต์ใช้ขั้วไฟฟ้ากราฟีนชนิดพิมพ์สกรีนที่ไม่ผ่านการดัดแปลงร่วมกับเทคนิคดิฟเฟอเรนเชียลพัลส์โวลแทมเมทรีในการวิเคราะห์ซัลไฟต์ในน้ำผลไม้บรรจุกล่อง อีกทั้งประเมินประสิทธิภาพของวิธีการที่พัฒนาขึ้นในด้านสภาพไวในการวิเคราะห์ ความแม่นยำ ความเที่ยงตรง และความเหมาะสมต่อการตรวจวิเคราะห์ในภาคสนาม
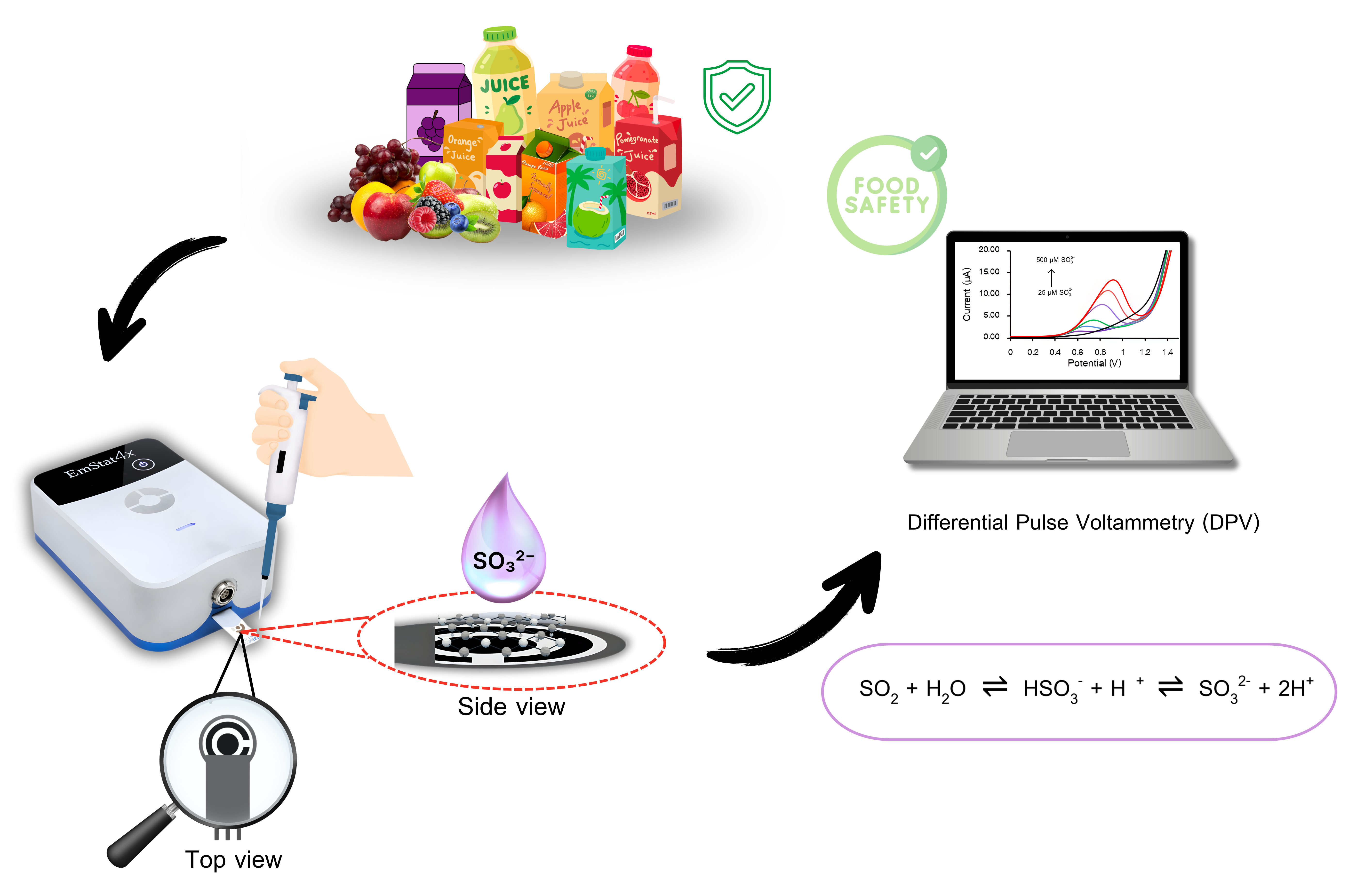
วิธีดำเนินงานวิจัย : การวิเคราะห์ซัลไฟต์ด้วยเทคนิคดิฟเฟอเรนเชียลพัลส์โวลแทมเมทรี (DPV) ภายใต้สภาวะที่เหมาะสม โดยการเตรียมสารละลายมาตรฐานซัลไฟต์ในช่วงความเข้มข้น 25 – 500 ไมโครโมลาร์ ตัวอย่างปริมาตร 80 ไมโครลิตร โดยกำหนดช่วงศักย์ไฟฟ้าที่ 0.00 – 1.50 โวลต์ สเตปโพเทนเชียล (step potential) 20 มิลลิโวลต์ มอดูเลชันแอมพลิจูด (modulation amplitude) 80 มิลลิโวลต์ มอดูเลชันไทม์ (interval time) 50 มิลลิวินาที และอินเทอร์วัลไทม์ (interval time) 200 มิลลิวินาที สำหรับการศึกษาพฤติกรรมทางไฟฟ้าเคมีของขั้วไฟฟ้าด้วยเทคนิคไซคลิกโวลเทมเมทรี สำหรับการศึกษาสภาวะที่เหมาะสมในการวิเคราะห์ ด้วยการศึกษาผลของพีเอชของสารละลายบัฟเฟอร์ และศึกษาพารามิเตอร์ของเทคนิคดิฟเฟอเรนเชียลพัลส์โวลแทมเมทรี ได้แก่ สเตปโพเทนเชียล (step potential) มอดูเลชันแอมพลิจูด (modulation amplitude) มอดูเลชันไทม์ (interval time) และอินเทอร์วัลไทม์ (interval time) โดยพิจารณากระแสไฟฟ้า และลักษณะสัญญาณที่เหมาะสมที่สุด นอกจากนี้ได้ศึกษาคุณลักษณะทางการวิเคราะห์ โดยศึกษาช่วงความเป็นเส้นตรง (linearity) ค่าขีดจำกัดต่ำสุดในการตรวจวัด (Limit of Detection: LOD) และขีดจำกัดในการวิเคราะห์ปริมาณ (Limit of Quantitation: LOQ) ศึกษาความเที่ยงในการวิเคราะห์จากความสามารถในการทำซ้ำ (Repeatability) และความสามารถในการทวนซ้ำ (Reproducibility) โดยแสดงในรูปของค่าร้อยละส่วนเบี่ยงเบนมาตรฐานสัมพัทธ์ (%RSD) สำหรับการศึกษาสารรบกวน อาทิ กรดแอสคอร์บิก กรดซิตริก โปแตสเซียมซอร์เบต และซูโครส เป็นต้น ทำโดยเลือกสารที่อาจพบในน้ำผลไม้ สำหรับการประยุกต์ใช้ในตัวอย่างจริง ได้นำตัวอย่างน้ำผลไม้ทั้งหมด 9 ชนิด ได้แก่ น้ำมะพร้าว น้ำแอปเปิล น้ำผักผลไม้รวม น้ำส้ม น้ำลิ้นจี่ น้ำลำไย น้ำฝรั่ง น้ำสตรอเบอร์รี่ และน้ำใบเตย จากซูเปอร์มาร์เก็ต โดยตัวอย่างแต่ละชนิดจะถูกนำมาวิเคราะห์ด้วยขั้วไฟฟ้ากราฟีน ชนิดพิมพ์สกรีนภายใต้สภาวะที่เหมาะสม
ผลการวิจัย : ขั้วไฟฟ้ากราฟีนชนิดพิมพ์สกรีน (SPGE) ให้กระแสไฟฟ้าสูงกว่าขั้วไฟฟ้าคาร์บอนพิมพ์สกรีน (SPCE) อย่างชัดเจน แสดงถึงสมบัติการนำไฟฟ้าที่ดีกว่าซึ่งสอดคล้องกับรายงานก่อนหน้าที่เกี่ยวข้องกับวัสดุกราฟีน นอกจากนี้ผลดังกล่าวยังสอดคล้องกับผลการวิเคราะห์ด้วยเทคนิคอิมพีแดนซ์สเปกโทรสโกปี (Electrochemical Impedance Spectroscopy: EIS) ที่พบว่าขั้วไฟฟ้ากราฟีนมีค่าความต้านทานการถ่ายเทประจุ (charge transfer resistance) ต่ำกว่า นอกจากนี้ได้ทำการศึกษาผลของค่าพีเอช (pH) ที่มีต่อลักษณะสัญญาณที่ตรวจวัดได้ของซัลไฟต์ พบว่าค่ากระแสไฟฟ้าเพิ่มขึ้นเมื่อพีเอชอยู่ในช่วง2.0 – 3.5 และลดลงเมื่อค่าพีเอชมากกว่า 5.5 ดังนั้นจึงเลือกพีเอชที่ 3.5 เป็นสภาวะที่เหมาะสมสำหรับการวิเคราะห์ต่อไป สำหรับพารามิเตอร์ของเทคนิคดิฟเฟอร์เรนเชียลพัลส์โวลเทมเมทรี (Differential Pulse Voltammetry: DPV) พบว่าพีกที่มีความสมมาตรและเสถียรที่สุดได้ภายใต้สภาวะการทดลอง คือ สเตปโพเทนเชียล 20 มิลลิโวลต์ มอดูเลชันแอมพลิจูด 80 มิลลิโวลต์ มอดูเลชันไทม์ 50 มิลลิวินาที และอินเทอร์วัลไทม์ 200 มิลลิวินาที ซึ่งจัดเป็นสภาวะที่เหมาะสมที่สุด และภายใต้สภาวะนี้ การวิเคราะห์ซัลไฟต์ให้ความเป็นเส้นตรงในช่วงความเข้มข้น 25 – 500 ไมโครโมลาร์ มีค่าสัมประสิทธิ์สหสัมพันธ์ (r²) เท่ากับ 0.9945 ค่าขีดจำกัดการตรวจวัด (LOD) และขีดจำกัดการวิเคราะห์เชิงปริมาณ (LOQ) มีค่าเท่ากับ 12.27 µM และ 40.92 µM ตามลำดับ และสำหรับการศึกษาสารรบกวนพบว่า ซูโครสมีผลรบกวนน้อยที่สุด ในขณะที่กรดแอสคอร์บิกมีผลรบกวนสูงที่สุด ทั้งนี้อาจเป็นเพราะกรดแอสคอร์บิกเป็นสารที่สามารถเกิดปฏิกิริยารีดอกซ์ได้ อย่างไรก็ตามพบว่าผลการรบกวนยังอยู่ในช่วงที่ยอมรับได้ และไม่ส่งผลกระทบต่อการวิเคราะห์ของวิธีวิเคราะห์ที่พัฒนาขึ้นนี้ได้ เมื่อนำวิธีนี้ไปประยุกต์ใช้กับน้ำผลไม้บรรจุกล่องจำนวน 9 ชนิด พบว่ามีค่าร้อยละการได้กลับคืนของซัลไฟต์อยู่ในช่วงระหว่างร้อยละ 80 – 120 แสดงให้เห็นว่าวิธี ที่พัฒนาขึ้นนี้มีศักยภาพที่จะนำไปใช้ในการวิเคราะห์ซัลไฟต์ในตัวอย่างจริงได้
สรุปผลการวิจัย : งานวิจัยนี้ได้พัฒนาวิธีการวิเคราะห์ซัลไฟต์ในเครื่องดื่มน้ำผลไม้โดยใช้เทคนิคดิฟเฟอร์เรนเชียลพัลส์ โวลแทมเมทรีร่วมกับขั้วไฟฟ้ากราฟีนชนิดพิมพ์สกรีนที่ไม่ผ่านการดัดแปลงใดๆ ภายใต้สภาวะที่เหมาะสมของสารละลายอิเล็กโทรไลต์ที่พีเอช 3.5 โดยวิธีที่พัฒนาขึ้นแสดงให้เห็นถึงประสิทธิภาพ และความน่าเชื่อถือสูง มีช่วงความเป็นเส้นตรงตั้งแต่ 25 – 500 ไมโครโมลาร์ (r² = 0.9945) ค่าขีดจำกัดการตรวจวัด และการวิเคราะห์เชิงปริมาณเท่ากับ 12.27 และ 40.92 ไมโครโมลาร์ ตามลำดับ ทั้งยังมีความเที่ยงที่ดีทั้งความสามารถในการทำซ้ำและการทวนซ้ำ โดยมีค่าร้อยละของส่วนเบี่ยงเบนมาตรฐานสัมพัทธ์อยู่ที่ร้อยละ 6.04 และ 5.68 ตามลำดับ การประยุกต์ใช้กับตัวอย่างน้ำผลไม้จริงให้ค่าร้อยละการได้กลับคืนอยู่ในช่วงร้อยละ 80 – 120 ซึ่งอยู่ในเกณฑ์มาตรฐานแสดงให้เห็นว่าวิธีที่พัฒนาขึ้นนี้มีความถูกต้อง แม่นยำ เสถียร และสามารถนำไปใช้ในการตรวจวิเคราะห์ซัลไฟต์ในผลิตภัณฑ์น้ำผลไม้ได้อย่างรวดเร็วและมีประสิทธิภาพ
เอกสารอ้างอิง
AOAC, I. (2016). Guidelines for Standard Method Performance Requirements (Appendix F), Official Methods of Analysis. Retrieved from https://www.aoac.org/
Arnold, B. C., Machado, E. d. S., Martins, J. B. L., Paterno, L. G., & Politi, J. R. d. S. (2025). Exploring the Electronic Structure of Graphene and Graphene Ultrathin Films with Adsorbed Lithium. The Journal of Physical Chemistry C, 129(16), 7879-7893. doi.org/10.1021/acs.jpcc.4c08241
Asangil, D., Hudai Tasdemir, I., & Kilic, E. (2012). Adsorptive stripping voltammetric methods for determination of aripiprazole. J Pharm Anal, 2(3), 193-199. doi.org/10.1016/j.jpha.2012.01.009
Candido da Silva, M. C., Cardoso Viana, A., Araujo Carvalho, A. J. B., Colombo Pimentel, T., Magnani, M., & Dos Santos Lima, M. (2024). Impact of sulfite use and acidification on chemical quality components in thermally processed watermelon juices. Food Res Int, 180, 114088. doi.org/10.1016/j.foodres.2024.114088
Codex Alimentarius, C. (2019). General Standard for Food Additives (CODEX STAN 192-1995). Retrieved from Retrieved from https://www.fao.org/gsfaonline/docs/CXS_192e.pdf
Ehsan, M. A., Khan, S. A., & Rehman, A. (2021). Screen-Printed Graphene/Carbon Electrodes on Paper Substrates as Impedance Sensors for Detection of Coronavirus in Nasopharyngeal Fluid Samples. Diagnostics (Basel), 11(6). doi.org/10.3390/diagnostics11061030
Gutema, K. F., Mekonnen, M. L., Yilma, B. T., Asrat, T. E., Dellith, J., Diegel, M., Csaki, A., & Fritzsche, W. (2025). Rapid Colorimetric Detection of Sulfite in Red Wine Using Alginate-Copper Laccase Nanozyme with Smartphone as an Optical Readout. ACS Meas Sci Au, 5(1), 145-154. doi.org/10.1021/acsmeasuresciau.4c00085
Jahani, P. M., Beitollahi, H., & Tajik, S. (2022). Surface amplification of graphite screen printed electrode using reduced graphene oxide/polypyrrole nanotubes nanocomposite; a powerful electrochemical strategy for determination of sulfite in food samples. Food Chem Toxicol, 167, 113274. doi.org/10.1016/j.fct.2022.113274
Joint, F. A. O. W. H. O. E. C. o. F. A. (2009). Evaluation of Certain Food Additives. Retrieved from https://apps.who.int/iris/handle/10665/43979
Karuwan, C., Wisitsoraat, A., Chaisuwan, P., Nacapricha, D., & Tuantranont, A. (2017). Screen-printed graphene-based electrochemical sensors for a microfluidic device [10.1039/C7AY00379J]. Analytical Methods, 9(24), 3689-3695. doi.org/10.1039/C7AY00379J
Kim, H. J. (1990). Determination of sulfite in foods and beverages by ion exclusion chromatography with electrochemical detection: collaborative study. J Assoc Off Anal Chem, 73(2), 216-222.
Kim, H. J., & Kim, Y. K. (2006). Analysis of Free and Total Sulfites in Food by Ion Chromatography with Electrochemical Detection. Journal of Food Science, 51, 1360-1361. doi.org/10.1111/j.1365-2621.1986.tb13122.x
Koch, M., Köppen, R., Siegel, D., Witt, A., & Nehls, I. (2010). Determination of Total Sulfite in Wine by Ion Chromatography after In-Sample Oxidation. Journal of Agricultural and Food Chemistry, 58(17), 9463-9467. doi.org/10.1021/jf102086x
Lee, D., Ro, H., Hwang, S., Lee, M., Kim, H., Heo, J., & Cha, S. (2024). Determination of Sulfites in Dried Fruits by Paper Spray Ionization Tandem Mass Spectrometry. Molecules, 29(10). doi.org/10.3390/molecules29102192
Lee, H. C., Liu, W.-W., Chai, S.-P., Mohamed, A. R., Aziz, A., Khe, C.-S., Hidayah, N. M. S., & Hashim, U. (2017). Review of the synthesis, transfer, characterization and growth mechanisms of single and multilayer graphene. RSC Advances, 7(26), 15644-15693. doi.org/10.1039/C7RA00392G
Lozer, T., Prezilius, A., dos Santos, G., Schaffel, I., Ramon Rosa, T., & Ferreira, R. (2022). ®®Development of a portable electroanalytical methodology for determination of sulfite in wine using screen-printed carbon electrodes modified with carbon nanotubes. Journal of Food Composition and Analysis, 116, 105052. doi.org/10.1016/j.jfca.2022.105052
Martins, P. R., Popolim, W. D., Nagato, L. A. F., Takemoto, E., Araki, K., Toma, H. E., Angnes, L., & Penteado, M. D. V. C. (2011). Fast and reliable analyses of sulphite in fruit juices using a supramolecular amperometric detector encompassing in flow gas diffusion unit. Food Chemistry, 127(1), 249-255. doi.org/10.1016/j.foodchem.2010.12.103
Mercy Magomya, A., Garbunga Yebpella, G., Chidinma Okpaegbe, U., John Oko, O., & Bature Gambo, S. (2020). Analysis and Health Risk Assessment of Sodium Benzoate and Potassium Sorbate in Selected Fruit Juice and Soft Drink Brands in Nigeria. International Journal of Pharmacy and Chemistry, 6(5). doi.org/10.11648/j.ijpc.20200605.11
Ministry of Public Health, & Food and Drug Administration. (2000). Ministry of Public Health Announcement No. 214 (2000) on Food Additives. Retrieved from https://food.fda.moph.go.th/law/data/announ_moph/214-43.pdf
Mohammadzadeh Jahani, P., Beitollahi, H., Tajik, S., Aflatoonian, M. R., Garkani Nejad, F., Zaimbashi, R., & Mohammadnavaz, A. (2024). CeO2 nanoparticles modified screen-printed carbon electrode: Electrochemical sensing platform for sulfite determination in water samples. International Journal of Electrochemical Science, 19(7). doi.org/10.1016/j.ijoes.2024.100621
Molinero-Abad, B., Alonso-Lomillo, M. A., Domínguez-Renedo, O., & Arcos, J. (2013). Amperometric determination of sulfite using screen-printed electrodes modified with metallic nanoparticles. Microchimica Acta, 180, 1351-1355. doi.org/10.1007/s00604-013-1074-8
Pasakon, P., Primpray, V., Thangphatthanarungruang, J., Kamsong, W., Wisitsoraat, A., Laiwattanapaisal, W., Intasanta, V., & Karuwan, C. (2024). Conductive disposable screen-printed graphene oxide-molybdenum disulfide electrode for electrochemical sensing applications. Electrochemistry Communications, 166.doi.org/10.1016/j.elecom.2024.107778
Pungjunun, K., Yakoh, A., Chaiyo, S., Siangproh, W., Praphairaksit, N., & Chailapakul, O. (2022). Smartphone-based electrochemical analysis integrated with NFC system for the voltammetric detection of heavy metals using a screen-printed graphene electrode. Mikrochim Acta, 189(5), 191. doi.org/10.1007/s00604-022-05281-x
Sartori, E., Takeda, H., & Fatibello-Filho, O. (2011). Glassy Carbon Electrode Modified with Functionalized Carbon Nanotubes Within a Poly(allylamine hydrochloride) Film for the Voltammetric Determination of Sulfite in Foods. Electroanalysis, 23. doi.org/10.1002/elan.201100122
Shaha, A., Esrafil, M., Akter, S., Bari, L., Khan, M. S. H., Alam, M. J., Dina, P. R., & Zubair, M. A. (2024). Determination of sodium benzoate in different brands of orange juices available in Bangladesh by high-performance liquid chromatography. Food Research, 8(1), 313-318. doi.org/10.26656/fr.2017.8(1).198
Silva, E. M., Takeuchi, R. M., & Santos, A. L. (2015). Carbon nanotubes for voltammetric determination of sulphite in some beverages. Food Chem, 173, 763-769. doi.org/10.1016/j.foodchem.2014.10.106
Verma, S. K., & Deb, M. K. (2007). Single-Drop and Nanogram Level Determination of Sulfite (SO32−) in Alcoholic and Nonalcoholic Beverage Samples Based on Diffuse Reflectance Fourier Transform Infrared Spectroscopic (DRS-FTIR) Analysis on KBr Matrix. Journal of Agricultural and Food Chemistry, 55(21), 8319-8324. doi.org/10.1021/jf071344c
Winiarski, J. P., de Barros, M., Magosso, H., & Jost, C. (2017). Electrochemical reduction of sulfite based on gold nanoparticles/silsesquioxane-modified electrode. Electrochimica Acta, 251. doi.org/10.1016/j.electacta.2017.08.171
Zhang, X., Liao, X., Wang, Y., Rao, L., & Zhao, L. (2024). Health effects of fruit juices and beverages with varying degrees of processing. Food Science and Human Wellness, 13(5), 2456-2479. doi.org/10.26599/fshw.2022.9250202
ดาวน์โหลด
เผยแพร่แล้ว
รูปแบบการอ้างอิง
ฉบับ
ประเภทบทความ
สัญญาอนุญาต
ลิขสิทธิ์ (c) 2026 คณะวิทยาศาสตร์ มหาวิทยาลัยบูรพา

อนุญาตภายใต้เงื่อนไข Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License.
Burapha Science Journal is licensed under a Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International (CC BY-NC-ND 4.0) licence, unless otherwise stated. Please read our Policies page for more information




